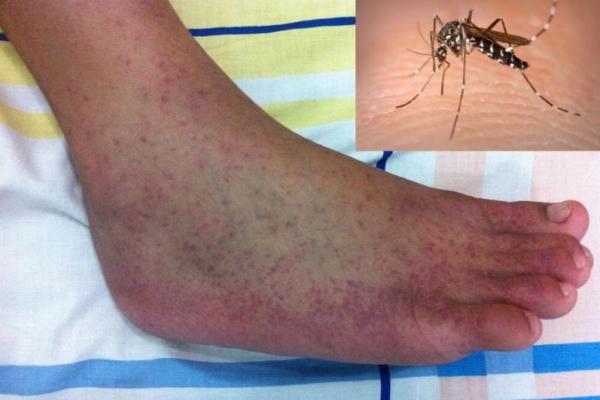
Poli Devi, yang putrinya Janvi termasuk di antara anak-anak yang meninggal setelah mengonsumsi sirup obat batuk yang terkontaminasi, di Ramnagar India, 28 Maret 2023. Foto: Reuters
NEW DELHI - Regulator obat India telah menemukan bahwa sirup obat batuk dan sirup antialergi yang dibuat oleh Norris Medicines (NORI.BO) beracun, menurut laporan pemerintah, beberapa bulan setelah sirup obat batuk buatan India diperkenalkan, terkait dengan 141 kematian anak di seluruh dunia.
Obat-obatan tersebut terkontaminasi dengan dietilen glikol (DEG) atau etilen glikol (EG), kontaminan yang sama yang ditemukan dalam sirup obat batuk yang menyebabkan kematian di Gambia, Uzbekistan dan Kamerun sejak pertengahan tahun lalu.
Ini adalah pertama kalinya dalam setidaknya dua tahun Organisasi Pengawasan Standar Obat Pusat (CDSCO) menandai adanya kontaminasi DEG dan EG dalam laporan bulanannya ketika negara tersebut mencoba menindak industri obat-obatan senilai $42 miliar yang didominasi oleh pemain kecil.
H.G. Koshia, komisaris Badan Pengawasan Obat dan Makanan negara bagian Gujarat, mengatakan kepada Reuters pada hari Rabu bahwa pihaknya telah memeriksa pabrik Norris bulan lalu dan memerintahkan pabrik tersebut untuk menghentikan produksi dan menarik kembali obat-obatan tersebut.
“Perusahaan gagal total dalam parameter kepatuhan praktik manufaktur yang baik,” kata Koshia. "Sistem air yang memadai tidak ada. Unit penanganan udara juga tidak memenuhi standar. Demi kepentingan kesehatan masyarakat yang lebih besar, kami memerintahkan unit tersebut untuk menghentikan produksi."
Managing Director Norris Vimal Shah menolak berkomentar di luar jam kerja.
Ekspektoran Trimax perusahaan mengandung 0,118% EG, sedangkan obat alergi Sylpro Plus Syrup mengandung 0,171% EG dan 0,243% DEG, menurut pengujian di laboratorium CDSCO, sesuai dengan daftar "kualitas tidak standar/palsu/dipalsukan/ obat salah merek" untuk bulan Agustus yang diunggah di situsnya. Koshia mengatakan Norris biasa mengekspor sirup obat batuk tersebut, namun tidak menyebutkan ke mana.
Organisasi Kesehatan Dunia (WHO) menyatakan batas aman berdasarkan standar yang diterima secara internasional tidak lebih dari 0,10%.
Belum jelas apakah obat-obatan Norris telah ditarik kembali atau menyebabkan bahaya. Kedua obat tersebut terdaftar di apotek online ketika Reuters memeriksanya.
CDSCO juga menemukan tiga batch sirup COLD OUT yang dibuat oleh Laboratorium Fourrts (India) yang terkontaminasi DEG dan EG. Organisasi Kesehatan Dunia mengatakan pada bulan Agustus bahwa sejumlah COLD OUT yang dijual di Irak memiliki tingkat DEG dan EG yang tidak dapat diterima.
Ketua Fourrts S.V. Veeramani tidak menanggapi permintaan komentar.
Veeramani, yang merupakan ketua Dewan Promosi Ekspor Farmasi India (pharmexcil) yang didukung pemerintah, mengatakan kepada Reuters pada bulan Agustus bahwa “analisis sampel retensi” COLD OUT baru-baru ini menunjukkan “tidak ada kontaminasi atau racun”.
“Belum ada laporan adanya efek buruk atau kematian akibat produk tersebut,” ujarnya melalui pesan WhatsApp. “Sebagai bentuk kehati-hatian, kami secara sukarela menarik kembali produk tersebut di pasar Irak.”
Peringatan mengenai obat-obatan beracun ini muncul ketika pemerintah, melalui pharmexcil, menyelenggarakan lokakarya bagi produsen obat di seluruh negeri untuk menekankan pentingnya kualitas obat dan keselamatan pasien.
Daftar CDSCO juga menyebutkan batch gliserin yang dibuat oleh Adani Wilmar (ADAW.NS), meskipun mengandung 0,025% EG, masih dalam batas keamanan WHO. Adani Wilmar tidak segera menanggapi permintaan komentar di luar jam kerja.
Para eksekutif dan regulator farmasi India mengatakan kepada Reuters bahwa merupakan praktik umum di antara beberapa produsen di negara tersebut untuk mengganti bahan-bahan yang lebih murah dan berkualitas komersial ketika membuat sirup obat batuk.
KEYWORD :Obat Sirup Gambia India Gagal Ginjal Akut